| TOPICO | INJURIA Y MUERTE CELULAR PARTE I |
| TIEMPO APROXIMADO | 45 MINUTOS |
| AUDIENCIA | ALUMNOS CURSO PATOLOGIA GENERAL, 2o año, Odontología, U Mayor |
| INSTRUCTOR | DR. BENJAMIN MARTINEZ R. |
- I. Racional
- II. Objetivos Terminales
- III. Objetivos Especificos
- IV. Test Inicial.
- Ciclo de Práctica I.
- Ciclo de Práctica II
- Ciclo de Práctica III
- Ciclo de Práctica IV
- Ciclo de Práctica V
I. RACIONAL:
La célula, o el tejido al recibir la acción de una injuria pueden morir, o sufrir una alteración morfológica o funcional. También pueden presentar una involución si falta la correcta nutrición. Así se puede producir atrofia, necrosis y alteraciones metabólicas que pueden afectar todos los órganos o tejidos del organismo.
II. OBJETIVOS TERMINALES:
El alumno podrá describir, clasificar y reconocer las principales características de atrofia, necrosis, apoptosis y gangrena.
III. OBJETIVOS ESPECIFICOS:
- Podrás definir y clasificar atrofia y necrosis.
- Serás capaz de describir las principales características morfológicas de órganos atróficos.
- Serás capaz de describir las características de las distintas variedades de necrosis y gangrena.
- Podrás señalar algunas características de la apoptosis.
CICLO DE PRACTICA I
Generalidades
Existe una serie de nombres para señalar las alteraciones ocasionadas por diversos agentes al actuar en un órgano, tejido o céula. En muchos textos se les denomina: Transtornos regresivos (Zollinger); Lesión y muerte celular (Robbins); Injuria celular y alteraciones del metabolismo (Anderson). Aschoff le llamaba distrofias y posteriormente se ha hablado de degeneraciones.
Hemos preferido simplificar el término Alteraciones Metabólicas, donde veremos algunos de los aspectos ocasionados por falta de nutrición (atrofia) y necrosis o muerte celular. Sobre estos dos temas nos referiremos en esta Unidad. En una segunda parte veremos procesos que generalmente se les ha llamado degeneraciones y ocasionados por alteraciones de aporte, síntesis o utilización de lípidos, proteínas, carbohidratos, agua y calcio.
El término atrofia, como hemos señalado, etimológicamente quiere decir «sin nutrición», pero en un órgano ya formado, generalmente se produce menor aporte sanguíneo, que causa una disminución de tamaño, ocasionado por disminución del número y tamaño de las células. La atrofia puede tener diverso origen : disminución de trabajo, fisiológica, falta de nutrición, pérdida de inervación, pérdida de estímulo endocrino, edad y debe distinguirse de hipoplasia en la que un órgano no se ha alcanzado a desarrollar completamente y por lo tanto tiene un menor tamaño, y es una respuesta de adapatación en la cual el órgano tiene menor tamaño por pérdida de sustancia celular.
Referencias bibliográficas
- Barahona R.: Lecciones de Patología General. Ed. Andrés Bello, Santiago, 1976, pags. 71-79.
Retroalimentación
1. Defina atrofia
2. A qué se debe la hipoplasia?
CICLO DE PRACTICA II
Atrofia
La atrofia representa una reducción en los componentes estructurales de la célula, tiene menos: mitocondrias, miofilamentos, y RE, pero generalmente aumentan las vacuolas autofágicas (estas vacuolas contienen componentes de fragmentos celulares). En general, un órgano atrófico se presenta disminuído de tamaño, color pardusco por la formación de un pigmento, lipofucsina, el que generalmente aumenta con la edad, por lo que es muy común de observar en la atrofia senil que afecta especialmente cerebro, hígado, corazón. Histológicamente se aprecia el pigmento en forma de gránulos amarillo parduzco cerca del núcleo. En el cerebro además de disminuir de tamaño, se produce hidrocéfalos externo e interno (lugares ocupados por líquido cefalo raquídeo).
También hay cierto grado de fibrosis en las leptomeninges y depósitos de lipofucsina en las neuronas. Este pigmento se cree que corresponde a focos de autodigestión celular. Estas verdaderas vacuolas autofágicas (con ME) contienen restos de RE, mitocondrias y lípidos.
Existen algunos órganos que una vez cumplida sus funciones involucionan, lo cual conocemos como atrofia fisiológica. Así ocurre en timo, ovario, este último se transforma en cuerpo fibroso durante la menopausia.
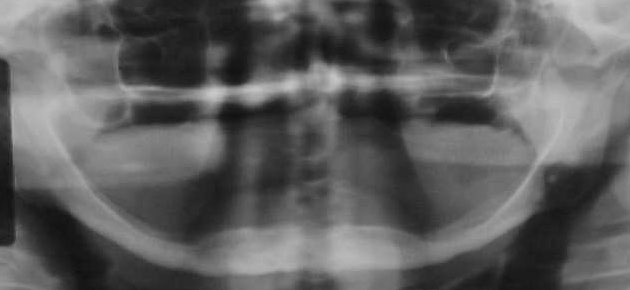
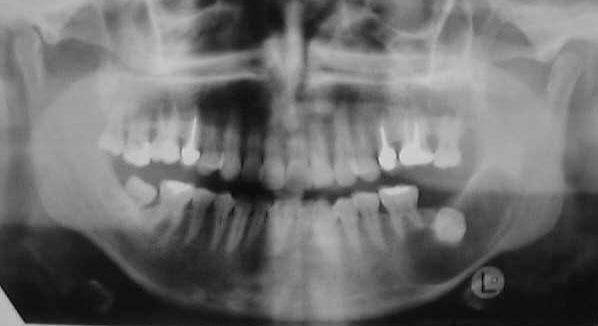
La falta de actividad en un órgano acostumbrado a ella, ocasiona atrofia, como en el músculo estriado y el hueso. En un hueso fracturado o en una parálisis al estar dichos tejidos inmovilizados durante largo tiempo disminuye su tamaño. Los huesos maxilares están acostumbrados también a recibir estímulos a través de los dientes, al faltar éstos, ocurre una reducción considerable del reborde alveolar, dificultando la restauración protésica. Igualmente en dientes que quedan sin sus antagonistas, se producen cambios atróficos en el hueso de soporte por inactividad.
Referencias Bibliográficas
- Zollinger H.U.: Anatomía Patológica. Patología General, Tomo I. Salvat Edit., Barcelona 1977, págs. 10-16.
Retroalimentación
1. Señale 3 tipos de atrofia.
2. La atrofia que afecta al timo se conoce como ____________ y generalmente se ha completado a los _____ años.
CICLO DE PRACTICA III
Necrosis
Necrosis es una de las expresiones de muerte celular, la otra es apoptosis, y se refiere a una serie de cambios morfológicos que acompañ a la muerte celular originados por la acción de enzimas. La reacción celular a una injuria depende del tipo, duración y severidad con que actúe. La que puede llegar a ocasionar la muerte celular, o antes de esta, una alteración de la función. La pérdida de la capacidad para generar ATP y proteínas no es suficiente para ocasionar la muerte celular en los hepatocitos, pero si al mantenerse durante cierto tiempo. El momento en que la sobrevida celular ya no es posible, se le llama punto de no retorno. Inmediatamente despues de la acción de una injuria, la célula en primer lugar pierde la capacidad para controlar su volumen, posteriormente acumula agua y más tarde gotitas de grasa en su citoplasma. Si el agente es letal, va a seguir la célula con fuertes movimientos de su membrana celular, formación de seudópodos anormales, e hinchazón del núcleo, luego picnosis (condensación de la cromatina), posteriormente disolución del núcleo por digestión enzimática (cariolisis) y finalmente citolisis.
La muerte celular por lo tanto, es un estado en que la célula no puede cumplir con ninguna función (secreción, motilidad, síntesis, absorción, reproducción, etc.). Inmediatamente despues de la muerte celular se liberan enzimas lisosomales, que destruyen el propio material celular y esta autodestrucción celular se denomina autolisis. En los tejidos con muchas enzimas es rapidísimo este proceso y muy grave como ocurre con páncreas y mucosa gástrica; es más lento en corazón, hígado y riñon y más lento en fibroblastos (o sea en tejidos conectivos).
Apoptosis
Poco se conoce acerca del proceso de muerte celular fisiológico, hoy en día conocido como apoptosis. La muerte celular programada puede tener una serie de influencias o responder a una serie de estimulos, algunos pueden estimularla y otros podrían inhibirla. En algunos tipos de cáncer, como linfomas, enfermedades autoinmunes (lupus eritematoso sisétmico) e infecciones virales (como la producida por el herpes) se cree que existe una inhibición de la apoptosis. Por otra parte en el SIDA, enfermedades neurodegenerativas como Alzheimer y Parkinson podría estar aumentada. La apoptosis se cree que también es responsable de una serie de fenómenos fisiológicos incluyendo: destrucción programada durante la embriogénesis, involución hormonal dependiente de la edad, muerte de células del sistema inmune (linfocitos T y B). Una diferencia importante con la necrosis es que la apoptosis no produce reacción inflamatoria en los tejidos, afecta a una o más células con condensación de la cromatina y formación de cuerpos apoptóticos (trozos de citoplasma con membrana), los cuales son fagocitados por células vecinas.
Referencias Bibliográficas
- Scarpelli D.G. and Chiga M.: Cell Injury and errors of metabolism in Anderson, W.A.D. and Kissane J.M.: Pathology 7th Ed. Vol. I Mosby, St. Louis, 1977, Ch. 3, pag. 92-98.
- Thompson CB. Apoptosis in the pathogenesis and treatment of disease. Science 267:1456, 1995.
- Necrosis de liquefacción, pulmón. WebPath – UTAH
- Apoptosis. WebPath – UTAH
- The Cell Death Society, APOPTOSIS.
Retroalimentación
1. El proceso autolítico en el tejido conjuntivo:
a) Es rápido, por la cantidad de fibras y su alto contenido de lisosomas en el fibroblasto;
b) Es rápido por la cantidad de células migratorias que a él llegan;
c) Es lento por la cantidad de células migratorias que a él llegan;
d) Es lento por la cantidad de fibras y bajo contenido de lisosomas en el fibroblasto.
2. Qué diferencias hay entre apoptosis y necrosis.
3. Nombre enfermedades donde aumenta y disminuye la muerte celular programada.
CICLO DE PRACTICA IV
Tipos de necrosis
De acuerdo a su aspecto macroscópico, la necrosis puede presentarse en dos formas principalmente:
- Necrosis de coagulación, generalmente causada por isquemia (falta de aporte sanguíneo), en que el órgano tiene un aspecto ópaco y seco. Dependiendo de su antiguedad tambien varía este aspecto, entre más reciente, más firme y pálida; a medida que avanza es más blanca y amarillenta. Con microscopio de luz se aprecian focos más eosinófilos que el tejido vecino. Puede verse esta necrosis en bazo, corazón y riñón. La causa más común es la isquemia, por lo tanto frecuente en infartos de dichos órganos se podrá observar (Fig. 3). Una variedad de esta necrosis es la caseificación (Fig. 4) que se presenta, especialmente en la tuberculosis como focos nodulares, amarillos, parecidos al queso, causada por productos lipídicos tóxicos de la pared del micobacterium.
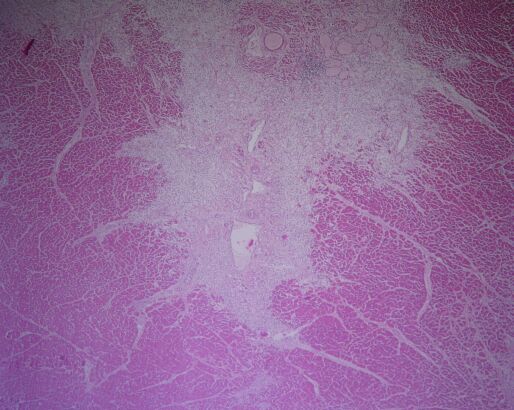


Fig. 3. Necrosis de coagulación, en infarto al miocardio. En a se observa miocardio separado por tejido menos teñido, más o menos de forma triangular. En b se aprecia hacia la derecha tejido muscular y a la izquierda el tejido disgregado, poco teñido, con algunos vasos prominentes. En c se puede apreciar mayor aumento con capilares y algunas células mononucleares con detritos nucleares. Tinción hematoxilina-eosina.

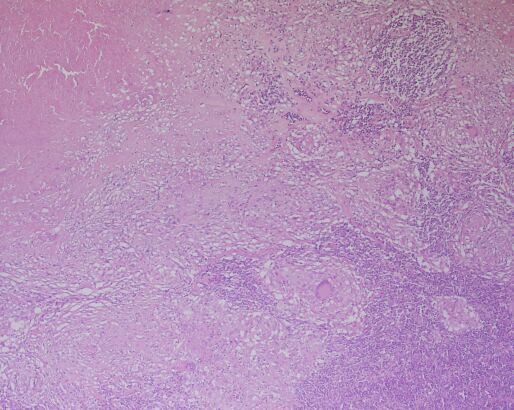
Fig. 4. Necrosis de caseificación. En ganglio tuberculoso se observa arriba a la izquierda (a), zona rojiza que denominamos a eso rojizo eosinofílico (todo lo teñido rojizo con HE es eosinofílico, todo lo azulado es basófilo). Hacia abajo se observa tejido linfático, y en el rincón inferior derecho cápsula. En b se observa mayor aumento del borde de la necrosis y la reacción granulomatosa con una célula de Langhans (hacia abajo a la derecha). Tinción hematoxilina eosina.
- Necrosis de liquefacción que quizás es la que más observamos, se forma rápidamente; por ejemplo, después de una quemadura en la piel al producirse una ampolla, en que tenemos un líquido seroso. En el SNC, después de un trauma violento, por isquemia grave puede presentarse y otro ejemplo es la necrosis presente en un absceso o sea el pus. En el abdomen, si se obstruye el conducto pancreático (por ejemplo por un cálculo biliar), puede el jugo pancreático, rico en lipasas, causar la necrosis del tejido adiposo vecino a dicho órgano, siendo muy graves las consecuencias de esta, conocida como Necrosis grasa.
Referencias Bibliográficas
- Scarpelli D.G. and Chiga M.: Cell Injury and errors of metabolism in Anderson, W.A.D. and Kissane J.M.: Pathology 7th Ed. Vol. I Mosby, St. Louis, 1977, Ch. 3, pag. 92-98.
Retroalimentación
1. ¿Qué cambios puede experimentar la necrosis por coagulación?
2. De tres ejemplos de necrosis por liquefacción:
a)
b)
c)
3. La necrosis por caseificación es una variedad de necrosis:
a) por liquefacción
b) de la grasa
c) coagulación
CICLO DE PRACTICA V
Gangrena
Este término se ha prestado para muchas confusiones con bacteriología: en el Diccionario de Ciencias Médicas Salvat, pág. 435, se define como «Mortificación de una parte del cuerpo producida por numerosas causas: físicas, químicas, circulatorias, nerviosas, tóxicas o infecciosas».
En la Patología de Anderson (Synopsis, pág. 60), dice que es un tejido necrótico en el cual existe putrefacción por invasión de bacterias saprófitas, pero por uso también se ha aplicado a áreas masivas de necrosis sin invasión de saprófitos, denominándose respectivamente gangrena húmeda y seca.
La gangrena de la extremidad inferior de un diábetico es uno de los ejemplos más conocidos, generalmente producida por isquemia y tenemos la gangrena isquémica, en que los tejidos primero se observan secos, amarillentos y posteriormente pardo-negruzcos. Si estos tejidos necróticos son invadidos por gérmenes saprófitos (gérmenes que viven a expensas de materia orgánica descompuesta), se produce putrefacción y así se habla de gangrena húmeda.
Si los gérmenes saprófitos que invaden los tejidos forman gases, como son los clostridium septicum, perfringens, etc., se habla de gangrena gaseosa; esta gangrena es muy grave y se produce muchas veces en la guerra o al sufrir heridas que se contaminan con tierra. Rápidamente se desarrolla la gangrena y el individuo puede fallecer si no es atendido prontamente. Los gérmenes clostridium al ser anaerobios, se multiplican en un ambiente con poco oxígeno y la infección y la destrucción de tejidos se produce por toxinas tales como lecitinasa. Tambien estos gérmenes producen gases, de ahí el nombre de esta gangrena ya que al presionar los tejidos suena como crepitación por dichos gases.
Referencias Bibliográficas
- Anderson W.A.D.; Scotti T. M.: Synopsis of Pathology. 9th Ed. Mosby, St., 1978, pag. 60, 187.
Retroalimentación
1. ¿Qué tipos de gangrena conoce?
a)
b)
c)
2. ¿Cuál es la causa de la gangrena?
3. Defina saprófito.
Mis opiniones acerca de esta Unidad
¿Algún comentario?, escriba a:
